8月28日,國際學術期刊Nature Communication在線發表了中國科學院上海生命科學研究院(營養與健康院)詹麗杏研究組的研究成果“Loss of Wwox drives metastasis in triple-negative breast cancer by JAK2/STAT3 axis”。該研究分析了三陰性乳腺癌患者的轉錄組特征,發現經典的IL6/JAK2/STAT3通路以及下游信號在三陰性乳腺癌中呈異常持續激活狀態,發現并確認了乳腺癌中JAK2/STAT3信號的新抑制子Wwox蛋白,闡明Wwox的異常減弱和JAK2/STAT3的異常激活這樣的負相關關系是高度惡性三陰性乳腺癌發生轉移的重要原因。
近年來,我國乳腺癌發病率持續上升,三陰性乳腺癌(triple negative breast cancer, TNBC)是其中惡性程度較高的類型。TNBC是指雌激素受體(ER)、孕激素受體(PR)和人表皮生長因子受體2(Her-2)均為陰性的一種乳腺癌亞型。三陰性乳腺癌侵襲力極強,遠處轉移風險大,預后極差。目前三陰性乳腺癌治療手段比較單一,以化療為主,極易復發和轉移。與其他類型乳腺癌相比,內分泌治療和分子靶向治療對三陰性乳腺癌均無效。如何為三陰性乳腺癌患者帶來更好的診斷手段和個性化治療選擇仍然是研究人員關注的重要問題。
帶著這一科學問題,詹麗杏研究組的研究人員篩選了三陰性乳腺癌細胞與正常乳腺細胞進行了轉錄組學分析,獲得IL6/JAK2/STAT3通路多個信號的異常表達特征。進一步采用人類細胞因子抗體芯片技術和體內體外模型,證明了三陰性乳腺癌細胞的IL6高度異常表達以及其激活的JAK2/STAT3的持續活化可能是三陰性乳腺癌發生遠端轉移的重要因素。研究中還發現,此前被認為的JAK2/STAT3的主要抑制因子SOCS3并未在三陰性乳腺癌中發揮其抑制作用;而我們新發現的脆性位點基因Wwox則在乳腺癌發生IL6/JAK2/STAT3信號通路持續活化過程中產生特異性抑制作用。通過采用NIH3T3/STAT3CA細胞模型,我們驗證了Wwox對體內持續STAT3信號高磷酸化水平以及持續活化狀態的抑制作用。此外結合雙熒光素酶報告基因法EMSA以及CHIP實驗,我們進一步驗證了Wwox蛋白可以抑制p-STAT3結合到IL-6啟動子區域從而抑制IL-6蛋白高表達。Wwox已被證實位于人類基因組中的常見型脆性位點(Common fragile sites,?CFSs),CFSs易于發生斷裂,從而影響相關功能基因的編碼。以往多篇文獻證明了Wwox在包括乳腺癌等多種腫瘤中的異常低表達。而我們基于體內體外以及臨床證據的研究證明相比其他類型乳腺癌,Wwox在三陰性乳腺癌中顯著低表達,且與IL6/JAK2/STAT3異常持續活化呈負相關關系。我們的研究首次證明了Wwox對腫瘤細胞JAK2/STAT3高磷酸化和持續活化的強抑制作用,而Wwox的作用機制有望為三陰性乳腺癌的個體化治療提供靶點和線索。
本研究由博士研究生常人緒等在詹麗杏研究員的指導下完成,也得到了以色列希伯來大學的Rami I. Aqeilan教授、盧森堡大學Claude Haan教授、中國科學院上海生化與細胞所王綱研究員的幫助。同時,本研究得到國家自然科學基金委,科技部以及中科院藥物先導等項目的共同資助以及上海營養與健康院公共技術平臺的支持。
原文鏈接:https://doi.org/10.1038/s41467-018-05852-8
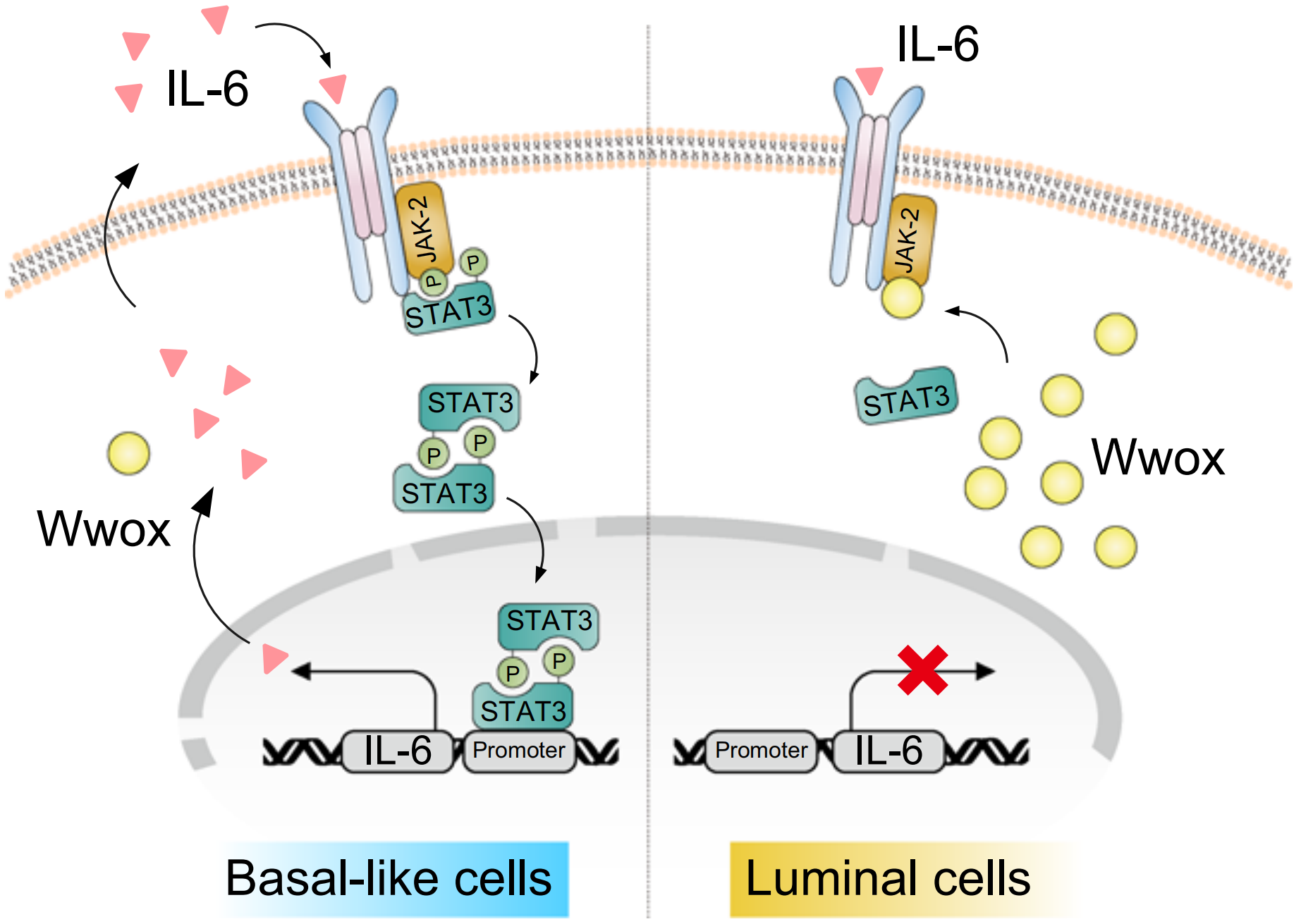
脆性位點基因Wwox作為抑制子在三陰性乳腺癌中與IL6/JAK2/STAT3通路持續活化呈負相關及其作用模式圖