近日,華東理工大學藥學院、生物反應器工程國家重點實驗室、光遺傳學與合成生物學交叉學科研究中心楊弋教授團隊與中國科學院上海營養與健康研究所科研團隊在蛋白質光遺傳學控制技術研究中取得突破性進展,在國際學術期刊《自然—通訊》上發表了題為“Controllingprotein stability with SULI, a highly sensitive tag for stabilization upon lightinduction”的研究文章。
?

?
基因編輯、轉錄調控和RNA干擾是目前廣泛應用的活細胞蛋白質操縱方法,可以用于研究特定蛋白在復雜生物過程中的功能。特別是CRISPR-Cas系統,其作為一種靈活和強大的基因組編輯工具,近年來得到了極為廣泛的應用。然而,這些技術均是在基因或mRNA水平對蛋白質進行控制,而mRNA轉錄生成和翻譯均需要時間,使得這些方法在表型控制方面存在有較大的延遲。內源性細胞蛋白可以在蛋白酶體靶向的情況下,通過蛋白酶體靶向的嵌合分子(PROTACs)或通過降解特定的抗體和抗體受體來進行快速降解。然而,發展這些蛋白特異的小分子誘導物或者抗體耗時較長且價格高昂,而且它們在生物體內自由擴散,一旦加入便很難從生物系統中去除,導致蛋白質調控的可逆性差。因此,發展可以直接在蛋白水平對蛋白質進行高時空分辨調控的工具是至關重要的。
光由于其精確的時間和空間分辨率可以滿足理想的蛋白質控制開關的幾乎所有要求。迄今為止,科學家們已經設計出了多種光誘導降解子(LIDs),并成功應用于酵母、線蟲、斑馬魚和哺乳動物細胞等模式生物中蛋白質降解的光遺傳學精密調控。已報道的LIDs均包括一個來自高等植物的藍光敏感LOV蛋白和一個C端降解子短肽(degron)。在黑暗條件下,LOV蛋白的C端α螺旋與它的核心結構域相互作用,從而將降解子短肽保護起來,不被蛋白酶識別和降解。在藍光照射下,LOV蛋白的C端α螺旋與LOV核心結構域解離,降解子短肽被釋放出來,進而被蛋白酶識別并降解。然而,這些LIDs即使在非誘導狀態下也會破壞目標蛋白的穩定性,從而縮小了蛋白質水平的動態調控范圍。此外,LIDs中的降解子短肽如鳥氨酸脫羧酶(ODC)的C端序列和四氨基酸小肽RRRG,只能在蛋白質的C端起作用。因此,LIDs必須融合在目標蛋白質的C端,因此對于不耐受C端融合的蛋白質來說并不適用。因此,發展具有優良光誘導特性且更好通用性的光敏感蛋白質降解子仍是非常急迫且具有挑戰性的。
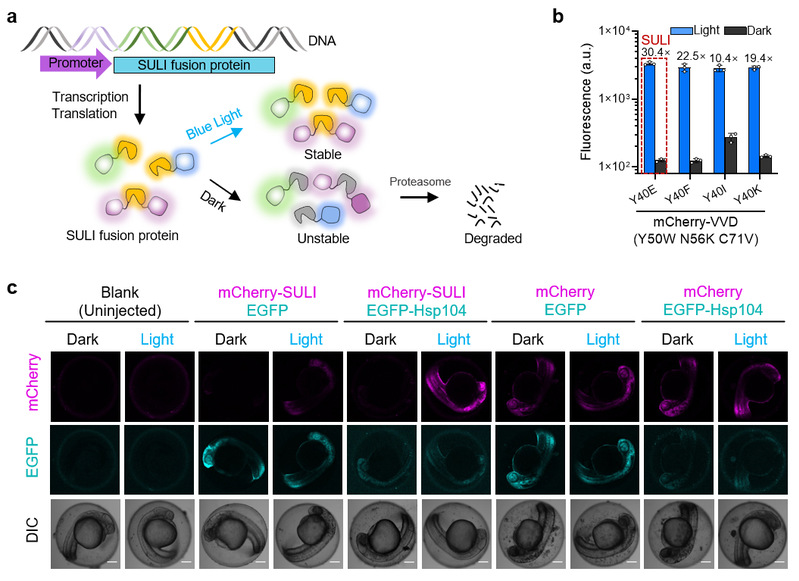
在本研究中,研究團隊基于光敏蛋白VVD發展了光誘導穩定的蛋白質降解標簽SULI(stabilization upon light induction)。在黑暗條件下,SULI標簽會被細胞的降解系統識別并降解;在藍光照射下,SULI標簽則非常穩定。實驗結果表明,SULI可被用于調控多種報告蛋白的穩定性。更重要的是,SULI可插入在目的蛋白的N端、C端甚至是內部來調控它們的穩定性。進一步研究結果表明,SULI對目的蛋白的降解是光強依賴的,并且可以震蕩式調控目的蛋白在細胞中的豐度。本研究還研究了SULI介導蛋白質降解的分子機制。結果表明,SULI是通過非賴氨酸泛素化依賴的蛋白酶體途徑降解的,并且還伴隨有聚集與去聚集過程。研究團隊利用顯微成像實驗證明SULI在其降解過程中會發生聚集,并在Hsp104蛋白的輔助下完成去聚集并進入蛋白酶體完成降解過程。本研究隨后利用SULI調控酵母細胞內源蛋白SicI的穩定性,實現酵母細胞周期的精確控制。此外,SULI還可用于調控斑馬魚中蛋白質的穩定性,通過對Pitx2蛋白穩定性的調控,本研究實現了斑馬魚發育過程的精確控制。綜上,SULI為研究不同細胞過程中的蛋白質代謝和功能提供了一個強大而方便的工具。
?
?
該篇論文第一作者為茅繆偉博士(現為中國科學院上海營養與健康所副研究員)、錢亞杰博士與張文耀博士,通訊作者為楊弋教授和陳顯軍教授。該研究獲得了中國科學院上海營養與健康所王澤峰研究員的大力支持。該研究得到了國家重點研發計劃、國家自然科學基金、上海市細胞代謝光遺傳學技術前沿科學研究基地、生物反應器工程國家重點實驗室基金、教育部基本科研業務費等經費資助。
原文鏈接:https://www.nature.com/articles/s41467-023-37830-0
?
?
來源:華東理工大學新聞網