2023年2月1日,中國科學院上海營養與健康研究所應浩研究組在Diabetes期刊在線發表了標題為“Adipocyte thyroid hormone β receptor-mediated hormone action fine-tunes the intracellular glucose and lipid metabolism and systemic homeostasis”的研究論文。該研究揭示了甲狀腺激素(thyroid hormone,TH)通過作用于白色脂肪組織(white adipose tissue,WAT)來調節全身代謝穩態。WAT中甲狀腺激素β受體(thyroid hormone receptor β,TRβ)通過靶向碳水化合物反應元件結合蛋白(carbohydrate response element binding protein,ChREBP)介導甲狀腺激素對多種代謝途徑的影響,而缺乏脂肪細胞TRβ的小鼠容易出現高脂飲食誘導的代謝異常,提示WAT中的TRβ可能是代謝性疾病的潛在靶點。
胰島素抵抗是2型糖尿病(type 2 diabetes,T2D)的主要致病因素,盡管骨骼肌是胰島素刺激葡萄糖攝取的主要部位,但有證據已表明,脂肪組織功能受損可導致胰島素抵抗以及增加T2D的風險。脂肪組織中葡萄糖攝取和脂肪酸從頭合成(de novo lipogenesis,DNL)的增加以及WAT的棕色化(browning)被認為對全身代謝功能具有改善作用。WAT棕色化產生的米色脂肪細胞(beige adipocytes),可以以線粒體解偶聯蛋白(uncoupling protein 1,UCP1)依賴或不依賴的方式促進能量耗散。白色和米色脂肪細胞之間的相互轉換伴隨著代謝重編程,其中涉及到控制葡萄糖和脂肪酸在細胞內的合成代謝和分解代謝途徑。揭示脂肪細胞各種代謝途徑的調控機制及相互作用,不僅可以更全面了解白色脂肪細胞米色化過程,而且可以為基于靶向脂肪細胞的代謝性疾病防治提供新策略和理論基礎。
甲狀腺激素在能量消耗和脂質代謝中至關重要,具有潛在的臨床應用前景。甲狀腺激素的作用主要是由其受體TR來實現的。甲狀腺激素通過與受體TR結合,轉錄調控相應基因的表達。TR具有TRα和TRβ兩種亞型,功能上具有組織特異性。甲狀腺激素如何協調脂肪細胞的各種代謝途徑,如何通過重塑脂肪細胞代謝調節全身代謝,尚不完全清楚。盡管早年就有甲狀腺激素調控脂肪組織基因表達的報道,但由于改變整體動物水平的甲狀腺激素水平會影響包括脂肪在內的其他組織的代謝,這給在體研究甲狀腺激素在脂肪組織內的生理功能帶來了挑戰。而利用組織特異的TR敲除小鼠探索甲狀腺激素組織特異的代謝調控功能可能是一種突破研究瓶頸的有益嘗試。
該研究發現甲狀腺激素的活性形式T3對全身代謝的有益作用伴隨著WAT細胞大小及棕色化在內的改變。利用脂肪細胞特異TRβ 敲除(ATRβKO)小鼠,發現TRβ可能是介導T3影響腹股溝WAT(inguinal WAT,iWAT)形態以及全身穩態的主要受體。進一步的基因表達分析提示,T3在iWAT中的作用包括促進葡萄糖利用(增加葡萄糖攝取和糖酵解),促進脂肪酸的合成代謝(包括脂肪酸從頭合成)和分解代謝(脂肪酸氧化),促進UCP1依賴和非依賴(無效代謝循環)的產熱,并由此增加機體的耗氧。而脂肪細胞TRβ的缺失可以消除T3的上述作用,提示T3對iWAT的糖脂代謝、產熱(棕色化)的調控,以及由此帶來的對全身穩態的影響,可以通過白色脂肪細胞的TRβ來實現。此外,通過分析附睪WAT(epididymal WAT,eWAT)和肩胛間棕色脂肪組織(interscapular BAT,iBAT),發現T3對eWAT的影響和iWAT有些類似,但對iBAT代謝途徑的影響相對小,提示iWAT是T3靶向的主要脂肪組織。
機制研究發現,在iWAT中T3以TRβ依賴的方式調控一個重要的轉錄因子ChREBP的表達。體外實驗提示,ChREBP介導了T3對糖脂代謝及能量代謝關鍵基因的表達。以往的研究提示,白色脂肪細胞ChREBP可通過促進胞內脂肪酸從頭合成,改善全身代謝,于是該研究還分析了脂肪細胞TRβ的缺失的后果。發現ATRβKO小鼠iWAT的脂肪酸從頭合成相關基因表達下調,更易發生飲食誘導的肥胖和代謝失調。該研究不但表明脂肪組織內的TH作用對于全身代謝穩態也具有調控作用,而且還揭示了脂肪TH-TRβ信號通路通過ChREBP調控脂肪細胞代謝和全身代謝的新機制,為靶向脂肪組織的TRβ激動劑的研發和臨床應用提供了理論基礎。
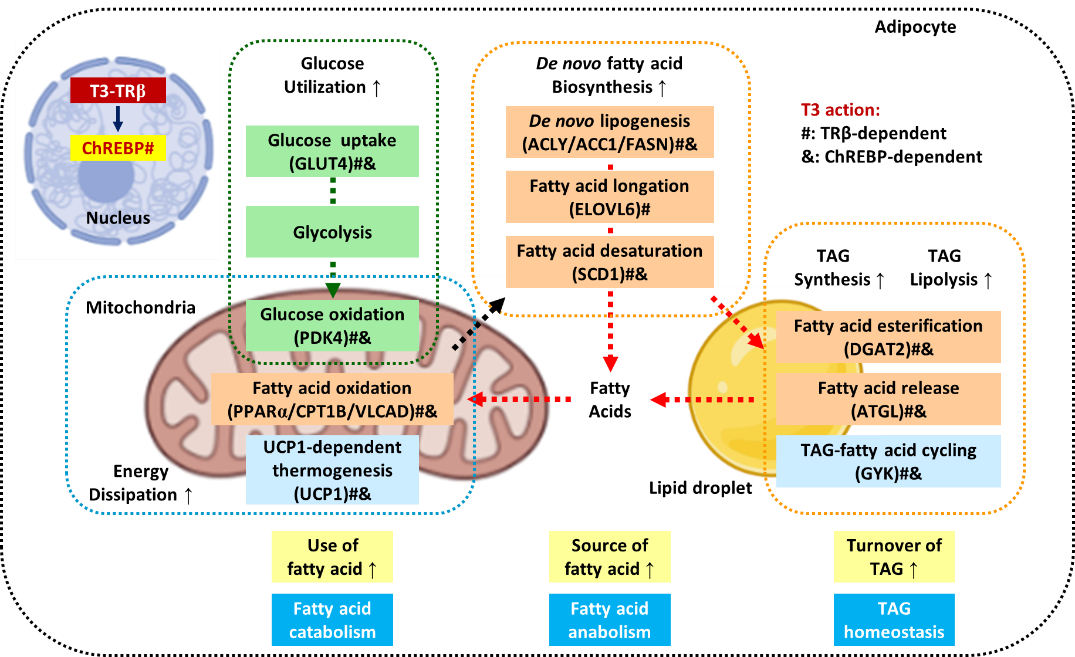
圖注:脂肪細胞甲狀腺激素信號通路對胞內代謝途徑的調控
中國科學院上海營養與健康研究所博士研究生馬伊若和沈思藝為該論文的共同第一作者,中科院上海營養與健康研究所應浩研究員,李俞瑩副研究員和復旦大學附屬醫院中山醫院蔣晶晶副主任醫師為本文的通訊作者。該研究得到了海軍軍醫大學章衛平教授等研究團隊的幫助以及國家自然科學基金委員會、中科院青促會、上海市科委的支持。