2022年8月16日,中國科學院上海營養與健康研究所丁秋蓉研究組在Journal of Hepatology期刊在線發表了標題為“MRG15 aggravates nonalcoholic steatohepatitis progression through regulating the mitochondrial proteolytic degradation of TUFM”的研究論文。該研究發現在NASH發生過程中,炎癥因子會增強MRG15的蛋白穩定性,而MRG15會在線粒體外膜與TUFM相互作用并下調TUFM的82和91賴氨酸位點乙酰化水平,從而促進TUFM被線粒體ClpXP蛋白酶體降解。肝臟中TUFM的減少會導致線粒體自噬受到抑制、氧化應激增加以及NLRP3炎癥小體的激活,加重炎癥和纖維化。在肝臟中敲除MRG15后可以顯著減緩小鼠NASH發展進程,該研究為NASH治療提供了潛在的靶點。
在21世紀,非酒精性脂肪肝病(nonalcoholic fatty liver disease, NAFLD)的全球發病率迅速增長,已經成為了最常見的慢性肝病。早期的NAFLD被稱為非酒精性脂肪肝(nonalcoholic fatty liver, NAFL),其病理特征為肝臟脂肪變性。當NAFLD發展到后期會成為非酒精性脂肪肝炎(nonalcoholic steatohepatitis, NASH),除了肝臟脂肪變性外還會有肝臟炎癥和纖維化出現。到了NASH階段不及時進行治療,就有可能繼續發展成肝硬化甚至肝細胞癌,嚴重威脅人類生命健康。NASH發病機制十分復雜,雖然有多款針對NASH的藥物在進行臨床試驗,但目前依舊沒有治療NASH的藥物被批準上市,因此深入探究NASH的發病機制和尋找NASH的潛在靶點對于NASH的治療至關重要。
致死因子4同源蛋白1(Mortality factor 4 like 1, MORF4L1)屬于MORF4家族,因為其位于人的第15號染色體上,所以也被稱為MRG15。MRG15被認為是一個定位在細胞核的表觀調控因子,參與在調控細胞增殖、DNA修復和胚胎發育過程。丁秋蓉研究組在前期工作中發現,MRG15可以節律性調控表觀染色質重塑和脂質合成進而促進高脂喂養誘導的小鼠肝臟脂肪變性(Nature metabolism?2020, 2(5):447-460)。然而,MRG15是否可以在NASH發展過程中參與調控炎癥和纖維化并不清楚。
在最新研究工作中,研究人員首先發現NASH小鼠肝臟和NASH患者肝臟中(商業化購得),MRG15蛋白水平發生上調,進一步探究發現在NASH發展過程中,炎癥因子可以通過上調MRG15的乙酰化水平進而增強MRG15的蛋白穩定性。當通過CRISPR技術在小鼠肝臟組織中敲除MRG15后可以顯著改善NASH小鼠肝臟脂肪變性、炎癥和纖維化情況,表明MRG15在NASH發展過程中發揮重要作用。通過與早期及后期NASH患者肝臟轉錄組比對分析發現,MRG15敲除后所改變的通路與在NASH患者后期失調的通路有更高的相關性,這些通路主要是炎癥和纖維化相關通路,然而炎癥和纖維化相關通路中的基因并不是MRG15直接靶向結合的基因,暗示著MRG15很有可能通過發揮獨立于表觀調控的功能影響炎癥和纖維化。
接下來,研究人員通過分離細胞組分發現MRG15不僅定位在細胞核中,還定位在細胞質和線粒體外膜上。通過CoIP-MS尋找MRG15相互作用蛋白發現,MRG15的確和一些線粒體定位蛋白存在相互作用,其中就包括線粒體Tu翻譯延伸因子(TUFM)。TUFM在之前的研究中被發現可以促進線粒體自噬和降低ROS,這對于NASH發展可能會起到保護作用。通過進一步探究發現,MRG15可以通過降低TUFM的82和91賴氨酸位點乙酰化水平進而加速TUFM被線粒體ClpXP蛋白酶體降解。而敲除MRG15后可以通過增強TUFM的蛋白穩定性進而促進線粒體自噬和降低ROS水平,從而減緩肝細胞損傷。有趣的是,TUFM在NASH患者的肝臟中也表現出明顯的降低,并且與MRG15的水平呈現顯著負相關,提示該機制同樣存在于NASH患者的發病過程中。
最后,為了探究MRG15對NASH的影響是否依賴于TUFM,研究人員在小鼠肝臟中同時敲除了MRG15和TUFM,發現MRG15和TUFM同時敲除后雖然可以改善NASH小鼠的肝臟脂肪變性,但是卻不能改善肝臟炎癥和纖維化情況,進一步表明MRG15在NASH發展過程中對肝臟脂肪變性的影響是依賴于其表觀調控脂合成基因表達的功能,而對炎癥和纖維化的影響則是依賴于對TUFM的蛋白穩定性調控。
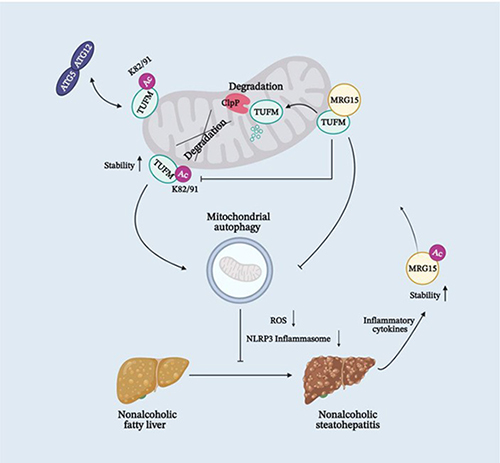
圖一:MRG15調控TUFM穩定性并促進NASH發展
綜上,該研究揭示了MRG15-TUFM軸對簡單的肝臟脂肪變性向NASH后期發展過程中所發揮的作用,并且發現該作用不依賴于MRG15的表觀重塑功能,為NASH治療提供了潛在的靶點。
中國科學院上海營養與健康研究所丁秋蓉研究員為該論文通訊作者,博士后田程為論文第一作者。這項工作得到了句容市人民醫院閔學文主任,中科院上海營養與健康研究所李于和周犇研究員,和香港中文大學Kathy O Lui教授的支持和幫助。該研究還得到了中國科學院上海營養與健康研究所公共技術平臺和動物平臺的支持。
文章鏈接:https://www.journal-of-hepatology.eu/article/S0168-8278(22)02981-6/fulltext